バナジウムの用途と酸化状態による用途
本コンテンツは、アディソン・ボイルによる2025年スタンフォード大学先端材料カレッジ奨学金申請からのものです。
はじめに
バナジウムは遷移金属に属し、その原子番号は23である。地殻中の存在量は亜鉛と同程度の0.02%である1。その存在量の多さにもかかわらず、過去50年まではあまり注目されていなかった。バナジウムには少なくとも6つ の異なる酸化状態があり、主に+3、+4、+5が存在する。V4+は青色、V3+は緑色、V2+は紫色である。3 これらの酸化状態は、生体システムにとって最も関連性の高いものでもある。
血液中のバナジウム:
このプロセスはpHに依存し、pHが上昇すると酸化還元電位は低下する。4薬剤として服用されると、バナジウムは血流に入り、血液中の血清成分に入る。
血漿には、V(III)の安定化につながる還元剤が存在する可能性があり、V(III)2- hTF種が形成される。血漿中のV(IV)Oが利用可能であれば、V(III)またはFe(III)がhTFに引き寄せられ、V(III)への還元がエネルギーの獲得から有利になる可能性がある。1V(III)の結合はlogK 20であり、V(IV)O+2の場合はlogK 13である。
バナジウムの他の酸化状態(V(IV)およびV(V))が配位子交換と酸化還元相互変換を起こす可能性があることが分かっている1。V(III)のように、V(IV)とV(V)がよく反応するのは、hTFのFe(III)結合部位の残基のためである1。V(IV)OSO4とapo-hTFをインキュベートした場合、hTFに対応することが示された。1また、生成比率はFe(III) 2hTFよりも低いことが示された。モノバナジン酸塩としてのV(V)とともに、VIVOおよびVIVO-担体錯体が、血中輸送物質であるholo-hTFに結合する可能性があることが分かっている。
バナジン酸塩:
バナジン酸塩:水溶液中でバナジン酸塩を用いる反応には、主に自己縮合反応、配位反応、酸化還元反応の3種類がある4。
縮合反応の場合、バナジン酸アニオンは弱酸性環境下でオリゴマーによってプロトン化され、より好ましい状態になる。4pHが様々なオルガネラにどのように影響するかという点から、これは細胞機能にとって極めて重要である。
バナジン酸塩はリン酸塩と類似しているため、バナジン酸塩は配位反応に使われ始めているが、まだ試験管の段階であり、ほとんどの配位反応は理論的なものである。 VO43-はPO43 -と構造的・電子的に類似している。図1.4バナジン酸錯体は5配位三角錐-両錐体型をしており、リン酸依存性酵素の反応で形成されると想定される5配位遷移状態と一致する。 4コンピューターモデリングでは、タンパク質を除くと、バナジン酸塩の大部分はH2VO4-とHVO42-の形をしていたが、タンパク質を含むと、バナジウムの大部分はトランスフェリンに結合していた。4 バナジン酸塩の金属錯体が配位子によって安定化されると、還元される可能性が高くなる。
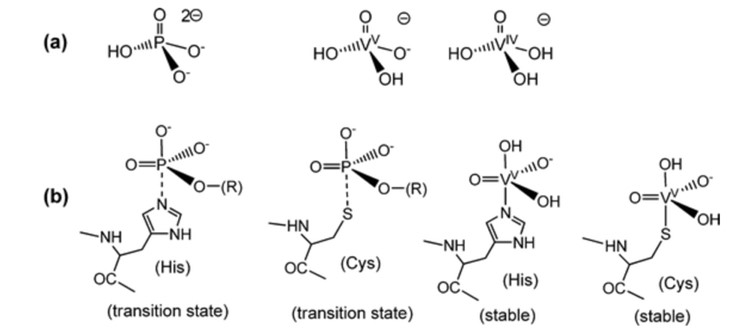
図1.リン酸塩とバナジン酸塩の遷移状態と安定性の比較5。
バナジン酸塩の還元のほとんどは、V(V)からV(IV)への還元であ る4。この種の反応は、さまざまな生体分子、特にオルガネラで起こる4。バナジウムが酵素の活性部位に結合すると、バナジン酸はリン酸のように容易に遊離しないため、糖尿病の治療に用いることができる。1バナジン酸を糖尿病の治療に用いるには、バナジウムによる酸化ストレス、世界的な毒性の問題、免疫系への影響、炎症などの欠点がある1。
がん研究:
バナジウムの特性は、がんとの闘いにおける化学療法の予防効果や抗腫瘍効果について研究されてきた。1試験は主に動物実験の段階と悪性細胞株で行われているようである。バナドセンジクロライドは水溶性で、pH7で塩化物イオンがH2Oに置換され、V(C5H5)2]2+となる。1DNAと結合し、シスプラチンと異なる挙動を示すことが確認されている。1また、毒性は限定的で、血液関門を通過することはなく、脳内では検出されない。バナジウムの抗がん作用のターゲットは、細胞代謝の阻害、シグナル伝達経路の阻害、細胞増殖の阻害である。1バナジウムの多様な反応と安全性については懸念があり、臨床研究が不足している。1-10-フェナントロリン誘導体を配位子とするV(IV)錯体やV(IV)O-dppz錯体は、特に白血病に対して抗がん作用を示している。
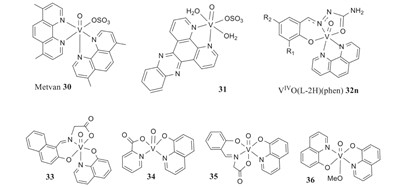
図2.図2 バナジン酸化合物の抗腫瘍性の描写(緩衝液の安定性はpH7.1
アマバジン
一般的なキノコのバナジウム含有量は0.5 mg kg-1未満だが、A. muscariaは100 mg V kg-1を含有することがある。バナジウム濃度が最も高いのは球根で、1000 mg V kg-1である。6この部分は菌柄の最下部に位置するため、土壌から最も汚染されやすい。表土を調べたところ、バナジウムの中央値は60mg kg-1で、その範囲は1.28~537mg kg-1であった6。電子常磁性共鳴(EPR)分光法によって、バナジウムの酸化状態が+4であることが発見された6。EPRスペクトルはまた、キノコの異なる部位に同じ化合物アマバジンが含まれていることも示していた6。バナジウム中心に配位することができる図3に示す2つの四座配位子は、合成アマバジンと天然アマバジンにほぼ等しく混在する2つの異性体を作り出す6。
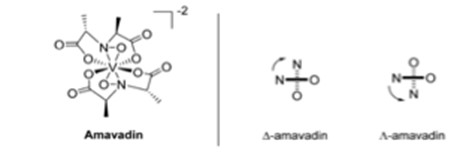
図3.アマバジンの構造(異性体DとLを含む)6。
アマバジンでは、V(IV)からV(V)への酸化は可逆的であり、これは触媒特性を持つ可能性があることを意味する6。 A.ムスカリアからアマバジンが合成されたとき、さまざまなバナジウム錯体が存在し、最も顕著なものは酢酸バナジルであることが判明した6。
結論
結論として、バナジウムは生物学的システムにおいて複数の用途があることが示されている。がん治療からキノコまで、その用途は多岐にわたる。研究では、さまざまな酸化状態と、血液や細胞などの生体系でどのように還元されるかが調べられてきた。バナジウムの主な酸化状態は+3、+4、+5であり、通常バナジウムと結びつく配位子は酸素錯体、特にバナジン酸塩と酢酸バナジルであった。バナジウムとそれが科学界に与える影響については、まだまだ研究が必要である。
参考文献
1. J.Costa Pessoa,Journal of Inorganic Biochemistry,2015, 147,4-24
2. A. Butler, and C. J. Carrano,Coordination Chemistry Reviews, 1991, 109, 61-65
3. D. Rehder,Bioinorganic Vanadium Chemistry, Wiley, Incorporated, New York, 2008.
4. X. Yang and K. Wang, Progress in Molecular and Subcellular Biology,eds.W. E. G. Muller, P. Jeanteur, R. E. Rhoads, D. Ugarkovic, and M. R. Custodio.Springer, Manz, Germany, 2013, ch. 1, pp 1-19.
5. D. Rehder,Metallomics,2015, 7, 732
6. S. Braeuer, M. Walenta, L. Steiner, and W. Goessler,Royal Society of Chemistry,2021, 36, 954-967.

 バー
バー
 ビーズと球体
ビーズと球体
 ボルト&ナット
ボルト&ナット
 坩堝
坩堝
 ディスク
ディスク
 繊維
繊維
 映画
映画
 フレーク
フレーク
 フォーム
フォーム
 フォイル
フォイル
 顆粒
顆粒
 ハニカム
ハニカム
 インク
インク
 ラミネート
ラミネート
 しこり
しこり
 メッシュ
メッシュ
 メタライズド・フィルム
メタライズド・フィルム
 プレート
プレート
 粉類
粉類
 ロッド
ロッド
 シーツ
シーツ
 単結晶
単結晶
 スパッタリングターゲット
スパッタリングターゲット
 チューブ
チューブ
 洗濯機
洗濯機
 ワイヤー
ワイヤー
 コンバータと計算機
コンバータと計算機
 Dr. Samuel R. Matthews
Dr. Samuel R. Matthews



